โครงการเศรษฐกิจพอเพียง พระราชดำริสำคัญๆมีอะไรบ้าง 14 โครงการ?
โครงการเศรษฐกิจพอเพียงมีอะไรบ้าง ตัวอย่างโครงการในพระราชดำริของในหลวง ร.9 ที่สำคัญมีอะไรบ้าง ประวัติของงานเกษตรแฟร์ วัตถุประสงค์งานเกษตรแฟร์
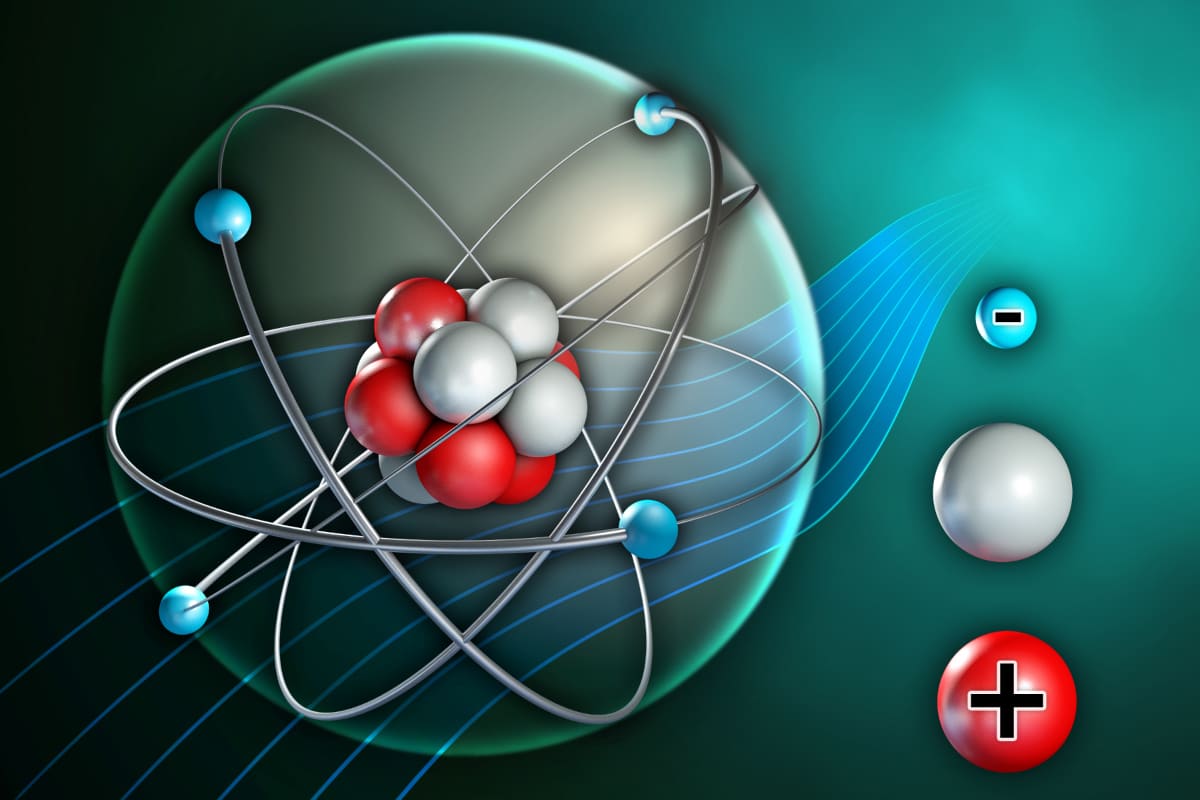
อะตอม
สสารประกอบด้วยอนุภาคที่เล็กที่สุดเรียกว่า อะตอม เนื่องจากอะตอมส่วนมากมีโครงสร้างที่เสถียร อะตอมจึงเป็นองค์ประกอบของทุกสิ่งในจักรวาล
โครงสร้างของอะตอม ตรงใจกลางหรือนิวเคลียสของอะตอมมีโปรตอน(ซึ่งมีประจุเป็นบวก) และนิวตรอน(ซึ่งไม่มีประจุ) อนุภาคที่มีประจุเป็นลบเรียกว่าอิเล็กตรอน ซึ่งโคจรรอบนิวเคลียสในแต่ละชั้นหรือเชลล์
เลชนิวคลีออน จำนวนโปรตอนและนิวตรอนทั้งหมดในนิวเคลียส คือ เลขนิวคลีออนของอะตอม
ไอโซโทป อะตอมของธาตุชนิดเดียวกันประกอบด้วยจำนวนโปรตอนเท่ากัน แต่ธาตุบางชนิดอาจมีจำนวนนิวตรอนต่างกัน เรียกธาตุนั้นว่า ไอโซโทป
การชนกันของอนุภาค นักวิทยาศาสตร์ค้นพบอนุภาคใหม่ๆ โดยการยิงอนุภาคที่เล็กกว่าอะตอมด้วยความเร็วสูง การชนกันทำให้เกิดอนุภาคใหม่ในช่วงสั้นๆ
ควาร์ก นิวตรอนกับโปรตอนประกอบด้วยอนุภาคที่เล็กกว่าเรียกว่า ควาร์ก ซึ่งเกาะติดกันด้วยอนุภาคเล็กเรียกว่า กลูออน “ดาวน์” ควาก์ มีประจุหนึ่งในส่ามของประจุลบ และ “อัป” ควาร์กมีประจุสองในสามของประจุบวก
ดีโมครีตัส ( นักปราชญ์ชาวกรีก) ได้กล่าวว่าทุกสิ่งทุกอย่างประกอบขึ้นจาก อนุภาคที่เล็กมาก เล็กมากจนไม่สามารถมองเห็นได้ อนุภาคเล็กๆ เหล่านี้จะรวมพวกเข้าด้วยกันโดยวิธิการต่างๆ สำหรับอนุภาคเองนั้นไม่มีการเปลี่ยนแปลงและไม่สามารถจะแตกแยกออกเป็นชิ้นส่วนที่เล็กลงไปอีกได้ ดีโมครี- ตัสตั้งชื่ออนุภาคนี้ว่า อะตอม (Atom) จากภาษากรีกที่ว่า atoms ซึ่งมีความหมายว่า ไม่สามารถแบ่งแยกได้อีก ตามความคิดเห็นของเขา อะตอมเป็นชิ้นส่วนที่เล็กที่สุดของสสารที่สามารถจะคงอยู่ได้
ภาพการแปรียบเทียบขนาดของอะตอม
1. ทราบสมบัติทางเคมีและสมบัติการเปล่งแสงของธาตุ
2. เราสามารถศึกษาแกแล็กซี่ (galaxy) ดวงดาวและดาวเคราะห์ต่างๆ โดยพิจารณาจากการศึกษาสเปกตรัมที่ได้จากดวงดาว
แบบจำลองอะตอมของจอห์นดอลตัน
จอห์น ดอลตัน นักวิทยาศาสตร์ชาวอังกฤษได้เสนอทฤษฎีอะตอมโดยอาศัยข้อมูลจากการทดลองที่พอจะศึกษาได้และนับว่าเป็นทฤษฎีแรกที่เกี่ยวกับอะตอมที่พอจะเชื่อถือได้ ซึ่งมีใจความดังนี้
จากทฤษฎีอะตอมของดาลตัน แบบจำลองอะตอมมีลักษณะดังรูป
ลักษณะแบบจำลองอะตอมของดอลตัน
( ตามทฤษฎีอะตอมของดอลตัน อะตอมในแนวคิดปัจจุบัน ข้อ 1, 3, 4 ใช้ไม่ได้ในปัจจุบัน)
ข้อ 1. อะตอมไม่ใช่สิ่งที่เล็กที่สุด อะตอมยังประกอบด้วยอนุภาคอิเล็กตรอน, โปรตอน, นิวตรอน เป็นต้น
ข้อ 3 – 4 อะตอมของธาตุชนิดเดียวกันมีคุณสมบัติทางกายภาพไม่เหมือนกัน กล่าวคือมีมวลไม่เท่ากัน ซึ่งจะได้กล่าวต่อไป ในเรื่อง ” ไอโซโทรป”
จากผลการทดลองของทอมสัน โกลด์สไตน์ ทำให้ทอมสันได้ข้อมูลเกี่ยวกับอะตอมมากขึ้นเขาจึงเสนอแบบจำลองอะตอมว่า
จากทฤษฎีอะตอมของทอมสัน แบบจำลองอะตอมมีลักษณะดังรูป
ลักษณะแบบจำลองอะตอมของทอมสัน
แบบจำลองอะตอมของรัทเทอร์ฟอร์ด
อะตอมจะประกอบด้วยนิวเคลียสที่มีโปรตอนและนิวตรอนรวมตัวกันอยู่อย่างหนาแน่นอยู่ตรงกลางนิวเคลียสมีขนาดเล็กมากมีมวลมาก และมีประจุบวกส่วนอิเล็กตรอนซึ่งมีประจุเป็นลบและมีมวลน้อยมาก จะวิ่งรอบนิวเคลียสเป็นวงกว้าง การค้นพบนิวตรอน เนื่องจากมวลของอะตอมส่วนใหญ่อยู่ที่นิวเคลียสซึ่งเป็นมวลของโปรตอนแต่โปรตอนมีมวลประมาณครึ่งหนึ่งของนิวเคลียสเท่านั้น แสดงว่าต้องมีอนุภาคซึ่งไม่มีประจุไฟฟ้าแต่มีมวลใกล้เคียงกับโปรตอนอยู่ในอะตอมด้วย เจมส์ แชวิก นักวิทยาศาสตร์ชาวอังกฤษ จึงศึกษาทดลองเพิ่มเติมจนพบนิวตรอนซึ่งเป็นกลางทางไฟฟ้า อะตอมของธาตุทุกชนิดในโลกจะมีนิวตรอนเสมอ ยกเว้นอะตอมของไฮโดรเจนในรูปของไอโซโทป
สรุปแบบจำลองอะตอมของรัทเทอร์ฟอร์ด อะตอมประกอบด้วยนิวเคลียสที่มีโปรตอนรวมกันอยู่ตรงกลาง นิวเคลียสมีขนาดเล็ก แต่มีมวลมากและมีประจุเป็นบวก ส่วนอิเล็กตรอนซึ่งมีประจุเป็นลบ และมีมวลน้อยมาก จะวิ่งอยู่รอบนิวเคลียสเป็นบริเวณกว้าง
จากทฤษฎีอะตอมของ รัทเทอร์ฟอร์ด แบบจำลองอะตอมมีลักษณะดังรูป
ลักษณะแบบจำลองอะตอมของรัทเทอร์ฟอร์ด
แบบจำลองอะตอมของนีลส์โบร์
นักวิทยาศาสตร์ได้พยายามศึกษาลักษณะของการจัดอิเล็กตรอนรอบๆ อะตอม โดยแบ่งการศึกษาออกเป็น 2 ส่วน ส่วนแรกเป็นการศึกษษเกี่ยวกับสเปกตรัมของอะตอม ซึ่งทำให้ทราบว่าภายในอะตอมมีการจัดระดับพลังงานเป็นชั้นๆ ในแต่ละชั้นจะมีอิเล็กตรอนบรรจุอยู่ ส่วนที่สองเป็นการศึกษาเกี่ยวกับพลังงานไอโอไนเซชัน เพื่อดูว่าในแต่ละระดับพลังงานจะมีอิเล็กตรอนบรรจุอยู่ได้กี่ตัว
สเปกตรัม หมายถึง อนุกรมของแถบสีหรือเส้นที่ได้จากการผ่านพลังงานรังสีเข้าไปในสเปกโตรสโคป ซึ่งทำให้พลังงานรังสีแยกออกเป็นแถบหรือเป็นเส้น ที่มีความยาวคลื่นต่างๆเรียงลำดับกันไป
นีลส์โบร์ ได้เสนอแบบจำลองอะตอมขึ้นมา สรุปได้ดังนี้
1 . อิเล็กตรอนจะเคลื่อนที่รอบนิวเคลียสเป็นชั้นๆ ตามระดับพลังงาน และแต่ละชั้นจะมีพลังงานเป็นค่าเฉพาะตัว
2. อิเล็กตรอนที่อยู่ใกล้นิวเคลียสมากที่สุดจะเรียกว่าระดับพลังงานต่ำสุดยิ่งอยู่ห่างจากนิวเคลียสมากขึ้น ระดับพลังงานจะยิ่งสูงขึ้น
3. อิเล็กตรอนที่อยู่ใกล้นิวเคลียสมากที่สุดจะเรียกระดับพลังงาน n = 1 ระดับพลังงานถัดไปเรียกระดับพลังงาน n =2, n = 3,… ตามลำดับ หรือเรียกเป็นชั้น K , L , M , N ,O , P , Q ….
จากทฤษฎีอะตอมของ นีลส์โบร์ แบบจำลองอะตอมมีลักษณะดังรูป
ลักษณะแบบจำลองอะตอมของนีลส์โบร์
แบบจำลองอะตอมแบบกลุ่มหมอก
เป็นแบบจำลองที่นักวิทยาศาสตร์คิดว่าเป็นไปได้มากที่สุดทั้งนี้ได้จากการประมวลผลการทดลองและข้อมูลต่างๆ อะตอมภายหลังจากที่นีลส์โบร์ ได้เสนอแบบจำลองอะตอมขึ้นมา อาจสรุปได้ดังนี้
1. อิเล็กตรอนไม่สามารถวิ่งรอบนิวเคลียสด้วยรัศมีที่แน่นอน บางครั้งเข้าใกล้บางครั้งออกห่าง จึงไม่สามารถบอกตำแหน่งที่แน่นอนได้ แต่ถ้าบอกได้แต่เพียงที่พบอิเล็กตรอนตำแหน่งต่างๆภายในอะตอมและอิเล็กตรอนที่เคลื่อนที่เร็วมากจนเหมือนกับอิเล็กตรอนอยู่ทั่วไป ในอะตอมลักษณะนี้เรียกว่า ” กลุ่มหมอก”
2. กลุ่มหมอกของอิเล็กตรอนในระดับพลังงานต่างๆจะมีรูปทรงต่างกันขึ้นอยู่กับจำนวนอิเล็กตรอน และระดับพลังงานอิเล็กตรอน
3. กลุ่มหมอกที่มีอิเล็กตรอนระดับพลังงานต่ำจะอยู่ใกล้นิวเคลียสส่วนอิเล็กตรอนที่มีระดับพลังงานสูงจะอยู่ไกลนิวเคลียส
4. อิเล็กตรอนแต่ละตัวไม่ได้อยู่ในระดับพลังงานใดพลังงานหนึ่งคงที่
5. อะตอมมีอิเล็กตรอนหลายๆระดับพลังงาน
ลักษณะแบบจำลองอะตอมแบบกลุ่มหมอก
สรุปแบบจำลองอะตอม
คำค้น : สรุป คือ pdf ppt ม.1 pdf ม.1 ppt ppt มหิดล doc ข้อสอบ เป็นการอธิบายที่อยู่ของอิเล็กตรอนในอะตอม ข้อสอบ พร้อมเฉลย ฟิสิกส์ แบบฝึกหัด ม. 1 การ์ตูน ทฤษฎีควอนตัมเบื้องต้น ประกอบด้วยอะไรบ้าง ม.4 ม.4 pdf ทฤษฎี มหาลัย pec9 ประกอบด้วย ภาษาอังกฤษ เป็นการอธิบายการอยู่ด้วยกันของอิเล็กตรอนในอะตอม เป็นการอธิบายการอยู่ด้วยกันของโปรตอนในอะตอม โจทย์ ข้อสอบ มีอะไรบ้าง แบบฝึกหัด เคมี ม.4 ข้อสอบ เคมี download โบร์ ม.1 แบบฝึกหัด หมายถึง สรุป แบบฝึกหัด ม. 4 แบบฝึกหัด pdf แบบฝึกหัด พร้อมเฉลย มหิดล
ที่มา:sites.google.com/a/kledlin.ac.th/kroonopporn14/raywicha-khemi-pheim-teim-1/xatxm-laea-tarang-thatu
อ่านบทความทั้งหมด >>> pangpond.com